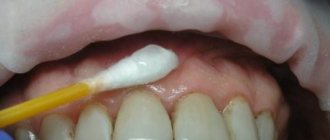
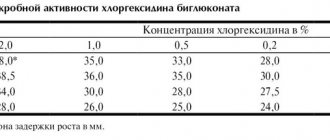
КЛАССИФИКАЦИЯ
Одонтогенные инфекции (инфекции полости рта), в зависимости от анатомической локализации, подразделяются на истинно одонтогенные
, связанные с поражением тканей зуба (кариес, пульпит);
пародонтальные
, связанные с поражением периодонта (периодонтит) и десны (гингивит, перикоронит), окружающих тканей (надкостницы, костной, мягких тканей лица и шеи, верхнечелюстного синуса, лимфоузлов);
неодонтогенные
, связанные с поражением слизистых оболочек (стоматит) и воспалением больших слюнных желез.
Данные виды инфекции могут быть причиной серьезных угрожающих жизни осложнений со стороны полости черепа, ретрофарингеальных, медиастинальных и других локализаций, а также диссеминированных гематогенным путем поражений клапанного аппарата сердца, сепсиса.
Гнойная инфекция лица и шеи
может быть неодонтогенного происхождения и включает фолликулит, фурункул, карбункул, лимфаденит, рожистое воспаление, гематогенный остеомиелит челюстей.
В челюстно-лицевой области также могут наблюдаться специфические инфекции (актиномикоз, туберкулез, сифилис, ВИЧ).
ОСНОВНЫЕ ВОЗБУДИТЕЛИ
Инфекции полости рта ассоциируются с постоянно присутствующей здесь микрофлорой. Обычно это смешанная флора, включающая более 3-5 микроорганизмов.
При истинно одонтогенной
инфекции, наряду с факультативными бактериями, прежде всего зеле-нящими стрептококками, в частности (
S.mutans, S.milleri
), выделяется анаэробная флора:
Peptostreptococcus
spp.,
Fusobacterium
spp.,
Actinomyces
spp.
При пародонтальной инфекции наиболее часто выделяют пять основных возбудителей: P.gingivalis, P.intermedia, E.corrodens, F.nucleatum, A.аctinomycetemcomitans
, реже
Capnocytophaga
spp.
В зависимости от локализации и тяжести инфекции, возраста пациента и сопутствующей патологии, возможны изменения в микробном спектре возбудителей. Так, тяжелые гнойные поражения ассоциируются с факультативной грамотрицательной флорой (Enterobacteriaceae
spp.) и
S.aureus
. У пациентов пожилого возраста и госпитализированных в стационар также преобладают
Enterobacteriaceae
spp.
В условиях отечественных бактериологических лабораторий достаточно сложно выделить специфического возбудителя определенной одонтогенной инфекции. Тем не менее, представляется возможным локализовать возбудителей, играющих основную роль в развитии инфекции полости рта, в наддесневом и поддесневом налете.
ПРИНЦИПЫ ЛЕЧЕНИЯ ИНФЕКЦИЙ ПОЛОСТИ РТА И ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ
Лечение одонтогенной инфекции
часто ограничивается местной терапией, включающей стандартные стоматологические манипуляции.
Системная антибактериальная терапия проводится только при распространении одонтогенной инфекции за пределы пародонта (под надкостницу, в кости, мягкие ткани лица и шеи), при наличии повышенной температуры тела, регионарного лимфаденита, интоксикации.
При выборе антимикробной терапии в условиях стационара, в случаях тяжелой гнойной инфекции, необходимо учитывать возможность присутствия резистентных штаммов среди таких анаэробов как Prevotella
spp.,
F.nucleatum
к пенициллину, что определяет назначение препаратов широкого спектра действия, амоксициллина/клавуланата в монотерапии или комбинации фторхинолона с метронидазолом. В связи с ростом уровня резистентности
Streptococcus
spp. к тетрациклину и эритромицину, данные препараты могут использоваться только как альтернативные. Так как отмечается умеренная активность метронидазола в отношении анаэробных кокков (
Peptostreptococcus
spp.), для повышения эффективности необходимо одновременное назначение β-лактамных антибиотиков.
Профилактическое системное применение АМП при выполнении стоматологических манипуляций в полости рта или периодонте не гарантирует уменьшения частоты инфекционных осложнений у соматически здоровых пациентов. Убедительных данных о достаточной эффективности местного применения антибиотиков при инфекциях полости рта не получено. В то же время бактерии полости рта являются резервуаром детерминант резистентности к АМП. Избыточное и неоправданное применение антибиотиков способствует их появлению и развитию резистентности патогенной микрофлоры.
ОДОНТОГЕННАЯ И ПАРОДОНТАЛЬНАЯ ИНФЕКЦИЯ
ПУЛЬПИТ
Основные возбудители
Зеленящие стрептококки (S.milleri
), неспорообразующие анаэробы:
Peptococcus
spp.,
Peptostreptococcus
spp.,
Actinomyces
spp.
Выбор антимикробных препаратов
Антимикробная терапия показана только в случае недостаточной эффективности стоматологических манипуляций или распространения инфекции в окружающие ткани (периодонт, периост и др.).
Препараты выбора
: феноксиметилпенициллин или пенициллин (в зависимости от тяжести течения).
Альтернативные препараты
: аминопенициллины (амоксициллин, ампициллин), ингибиторозащищенные пенициллины, цефаклор, клиндамицин, эритромицин + метронидазол.
Длительность применения
: в зависимости от тяжести течения (не менее 5 дней).
ПЕРИОДОНТИТ
Основные возбудители
В структуре периодонта микрофлора выявляется редко и обычно это S.sanguis, S.oralis, Actinomyces
spp.
При периодонтите у взрослых преобладают грамотрицательные анаэробы и спирохеты. P.gingivalis, B.forsythus, A.аctinomycetemcomitans и T.denticola
выделяются наиболее часто.
В ювенильном возрасте наблюдается быстрое вовлечение в процесс костной ткани, при этом обычными возбудителями являются A.аctinomycetemcomitans
и
Capnocytophaga
spp.
P.gingivalis
выделяется редко.
У пациентов с лейкемией и нейтропенией после химиотерапии наряду с A.actinomycetemcomitans
выделяется
C.micros
, а в препубертатном возрасте —
Fusobacterium
spp.
Выбор антимикробных препаратов
Препараты выбора
: доксициклин; амоксициллин/клавуланат.
Альтернативные препараты
: спирамицин + метронидазол, цефуроксим аксетил, цефаклор + метронидазол.
Длительность терапии
: 5-7 дней.
Пациентам с лейкемией или нейтропенией после химиотерапии применяются цефоперазон/сульбактам + аминогликозиды; пиперациллин/тазобактам или тикарциллин/клавуланат + аминогликозиды; имипенем, меропенем.
Длительность терапии
: в зависимости от тяжести течения, но не менее 10-14 дней.
ПЕРИОСТИТ И ОСТЕОМИЕЛИТ ЧЕЛЮСТЕЙ
Основные возбудители
При развитии одонтогенного периостита и остеомиелита в 50% случаев выделяется S.aureus
, а также
Streptococcus
spp., и, как правило, превалирует анаэробная флора:
P.niger, Peptostreptococcus
spp.,
Bacteroides
spp. Реже выявляются специфические возбудители:
A.israelii, T.pallidum
.
Травматический остеомиелит чаще обусловлен наличием S.aureus
, а также
Enterobacteriaceae
spp.,
P.aeruginosa
.
Выбор антимикробных препаратов
Препараты выбора
: оксациллин, цефазолин, ингибиторозащищенные пенициллины.
Альтернативные препараты
: линкозамиды, цефуроксим. При выделении
P.aeruginosa
— антисинегнойные препараты (цефтазидим, фторхинолоны).
Длительность терапии
: не менее 4 нед.
ОДОНТОГЕННЫЙ ВЕРХНЕЧЕЛЮСТНОЙ СИНУСИТ
Основные возбудители
Возбудителями одонтогенного верхнечелюстного синусита являются: неспорообразующие анаэробы — Peptostreptococcus
spp.,
Bacteroides
spp., а также
H.influenzae, S.pneumoniae
, реже
S.intermedius, M.сatarrhalis, S.pyogenes
. Выделение
S.aureus
из синуса характерно для нозокомиального синусита.
Выбор антимикробных препаратов
Препараты выбора
: амоксициллин/клавуланат. При нозокомиальной инфекции — ванкомицин.
Альтернативные препараты
: цефуроксим аксетил, ко-тримоксазол, ципрофлоксацин, хлорамфеникол.
Длительность терапии
: 10 дней.
Обработка стоматологического инструментария
К обработке стоматологического инструментария санитарное законодательство выдвигает строгие требования, которые должны выполнять все без исключения стоматологические кабинеты вне зависимости от формы собственности. Такие высокие требования совершенно обоснованы, ведь стоматологические инструменты могут травмировать слизистую оболочку полости рта, что связано с высоким риском заражения инфекциями.
Для бесперебойной работы стоматкабинета необходимо иметь достаточное количество стерильных инструментов, не менее десяти наборов на каждого врача на смену. Такой подход позволит обслужить большое количество пациентов и при этом успевать планомерно обрабатывать использованный инструментарий.
Согласно требованиям санитарного законодательства стоматологические инструменты должны обрабатываться в три этапа:
- Дезинфекция;
- Предстерилизационная обработка;
- Стерилизация.
Дезинфекция стоматологических инструментов
Итак, первым этапом обработки инструментов является дезинфекция, которая призвана максимально снизить уровень контаминации микроорганизмами инструментов. Дезинфекция осуществляется с использованием дезинфицирующих средств. К выбору дезсредства нужно подойти ответственно. Дезинфицирующее средство, во-первых, должно эффективно уничтожать микроорганизмы и во-вторых, не портить инструменты. Этим свойствам в полной мере отвечают дезинфицирующие средства для стоматологий «Септолит Тетра» и «Септолит Денталь».
Дезинфекцию инструментов проводят после каждого клиента. Для этого в емкость с дезсредством погружают использованные инструменты в раскрытом и разобранном виде. Уровень жидкость должен полностью покрывать инструменты. Дезинфекцию необходимо проводить по режиму, применяемому при вирусных инфекциях.
По окончанию времени выдержки приступают к предстерилизационной очистке, которая проводится с целью очищения инструментов от белковых загрязнений. Средства «Септолит Тетра» и «Септолит Денталь» позволяют совместить дезинфекцию и ПСО в один этап. Поэтому после окончания дезинфекции прямо в контейнере с дезсредством проводят тщательное очищение инструментов с помощью щеточек.
Дезинфекцию оттисков и заготовок протезов проводят перед их отправлением в зубочелюстную лабораторию и перед установкой пациенту. После дезобработки оттиски и протезы промывают дистиллированной водой. На этом обработка этих стоматологических изделий окончена.
Стерилизация инструментов
Все изделия, контактирующие с кровью и раневой поверхностью, которые могут приводить к травмированию слизистой, должны подвергаться стерилизации. Обработку стоматологического инструментария проводят с помощью паровой или воздушной стерилизации. Для этого продезинфицированный инструментарий помещают в упаковку (бумажные пакеты или контейнеры) и отправляют в стерилизатор. Стерилизацию в автоклаве проводят в течение 20 минут при температуре 132 °С, в сухожаровом шкафу в течение 60 минут при температуре 180 °С.
Стерильный инструментарий хранят в запакованном виде в крафт-пакетах, а в распакованном виде — в УФ-стерилизаторах. Обратите внимание, что стерильный инструментарий ассистент должен выкладывать на столик непосредственно перед началом манипуляции.
Согласно санитарному законодательству химическая стерилизация с применением дезсредств допускается лишь в тех случаях, когда другие методы стерилизации применить невозможно. Это касается стерилизации инструментов, изготовленных из термолабильных материалов. Химическую стерилизацию проводят строго с соблюдением правил антисептики. После завершения химической стерилизации инструменты промывают дистиллированной водой.
ГНОЙНАЯ ИНФЕКЦИЯ МЯГКИХ ТКАНЕЙ ЛИЦА И ШЕИ
Основные возбудители
Гнойная одонтогенная инфекция мягких тканей лица и шеи, клетчатки глубоких фасциальных пространств ассоциируется с выделением полимикробной флоры: F.nucleatum
, пигментированными
Bacteroides, Peptostreptococcus
spp.,
Actinomyces
spp.,
Streptococcus
spp.
АБСЦЕССЫ, ФЛЕГМОНЫ ЛИЦА И ШЕИ
Основные возбудители
При абсцессе в области орбиты у взрослых выделяется смешанная флора: Peptostreptococcus
spp.,
Bacteroides
spp.,
Enterobacteriaceae
spp.,
Veillonella
spp.,
Streptococcus
spp.,
Staphylococcus
spp.,
Eikenella
spp.. У детей превалируют
Streptococcus
spp.,
Staphylococcus
spp.
Возбудителями абсцессов и флегмон неодонтогенного происхождения, чаще обусловленных мелкими повреждениями кожи, являются S.aureus, S.pyogenes
.
При гнилостно-некротической флегмоне дна полости рта выделяется полимикробная флора, включающая F.nucleatum, Bacteroides
spp.,
Peptostreptococcus
spp.,
Streptococcus
spp.,
Actinomyces
spp. Кроме названных, у пациентов с тяжелым течением могут быть выделены грамотрицательные бактерии и
S.aureus
(чаще у пациентов, страдающих сахарным диабетом и алкоголизмом).
Выбор антимикробных препаратов
Препараты выбора:
ингибиторозащищенные пенициллины (амоксициллин/клавуланат, ампициллин/сульбактам), цефоперазон/сульбактам.
При выделении P.aeruginosa
— цефтазидим + аминогликозиды.
Альтернативные препараты:
пенициллин или оксациллин + метронидазол, линкозамиды + аминогликозиды II-III поколения, карбапенемы, ванкомицин.
Длительность терапии:
не менее 10-14 дней.
БУККАЛЬНЫЙ ЦЕЛЛЮЛИТ
Основные возбудители
Обычно наблюдается у детей в возрасте до 3-5 лет. Основным возбудителем является H.influenzae
тип В и
S.pneumoniae
. У детей в возрасте до 2 лет
H.influenzae
— основной возбудитель, при этом, как правило, наблюдается бактериемия.
Выбор антимикробных препаратов
Препараты выбора
: амоксициллин/клавуланат, ампициллин/сульбактам, цефалоспорины III поколения (цефотаксим, цефтриаксон) в/в, в высоких дозах.
Альтернативные препараты
: хлорамфеникол, ко-тримоксазол.
Длительность терапии
: в зависимости от тяжести течения, но не менее 7-10 дней.
ЛИМФАДЕНИТ ЛИЦА И ШЕИ
Основные возбудители
Регионарный лимфаденит в области лица и шеи наблюдается при инфекции в полости рта и лица. Локализация лимфаденита в поднижнечелюстной области, по передней и задней поверхности шеи у детей в возрасте 1-4 лет, как правило, связана с вирусной инфекцией.
Абсцедирование лимфоузлов обычно обусловлено присоединением бактериальной инфекции. При одностороннем лимфадените по боковой поверхности шеи у детей старше 4 лет в 70-80% выделяются БГСА и S.aureus
. Анаэробные возбудители, такие как
Bacteroides
spp.,
Peptococcus
spp.,
Peptostreptococcus
spp.,
F.nucleatum, P.acnes
, могут быть причиной развития одонтогенного лимфаденита или воспалительных заболеваниях слизистой оболочки полости рта (гингивит, стоматит), целлюлита.
Выбор антимикробных препаратов
Препараты выбора: АМП, соответствующие этиологии первичного очага инфекции.
Чрезвычайная значимость инфекционной патологии в современном мире с его высокой мобильностью и экономической взаимозависимостью заключается в ее глобальной опасности для общественного здравоохранения каждой отдельно взятой страны и всего мирового сообщества в целом. Проведенная международными экспертами ВОЗ комплексная оценка рисков для здоровья населения, вызванных инфекционными агентами, позволила прийти к заключению, что нынешняя ситуация в мире далека от стабильности. Рост населения, стремительная урбанизация и глобализация, ухудшение состояния окружающей среды, быстрое внедрение в практику новых форм оказания медицинской помощи и необоснованное масштабное применение противомикробных препаратов привели к нарушению хрупкого равновесия в микробиологическом сообществе. На рубеже XX-XXI веков мы стали свидетелями беспрецедентных в истории темпов появления «новых» болезней (минимум по 1 нозологии в год!), распространения инфекционных болезней с атипичными клиническими проявлениями (25-57%) и «возвращающихся» инфекций (дифтерия, туберкулез, сифилис и др.), что, безусловно, и определило остроту проблемы инфекционной безопасности в современном мире [2, 22].
По нашему твердому убеждению, найти решение этой проблемы можно лишь сообща с привлечением специалистов из разных областей знаний. Ведь сущность инфекционной патологии как медицинской проблемы заключается не только в риске эпидемий и утяжелении течения острых инфекционных болезней. Сегодня ни для кого не секрет, что на первый план выходят длительно персистирующие инфекции со скудными клиническими проявлениями, возбудители которых выполняют этиологическую или триггерную роль в развитии гематологических, онкологических, неврологических, стоматологических заболеваний, поражения почек, печени, суставов и др. [7, 8, 12, 15-18, 21, 23]. Необходимость глубокого понимания вопросов инфекционной патологии и инфекционной безопасности врачами различных специализаций — насущная, жизненно важная проблема.
С этой точки зрения стоматологи занимают особую нишу, если учесть распространенность стоматологических заболеваний среди лиц всех возрастных групп (56-99% населения) и массовость обращений населения за стоматологической помощью. Уникальный количественный и качественный состав микрофлоры полости рта и интенсификация современной стоматологии чрезвычайно повышают риск перекрестного инфицирования пациентов и профессионального заражения медицинских работников. Достичь санитарно-эпидемиологического благополучия в медицинских стоматологических учреждениях поликлинического и стационарного уровня можно лишь объединив усилия стоматологов и инфекционистов в изучении инфекционно-ассоциированной патологии. Это в полной мере перекликается с утверждением American dental association (2012): «Стоматологическое обслуживание является неотъемлемым компонентом общего здравоохранения. Повышая качество стоматологических услуг, мы улучшаем общественное здоровье и благосостояние нации».
В настоящее время доля лиц с отягощенным преморбидным фоном среди пациентов стоматологов достигает 93,3%. Наиболее часто среди них встречаются лица с инфекционной патологией (острыми и хроническими гнойно-септическими заболеваниями, вирусными гепатитами, герпесвирусной инфекцией, ВИЧ-инфекцией, микозами и др.), пищевой и лекарственной аллергией, часто болеющие острыми респираторными вирусными инфекциями (ОРВИ) и пр. Причем в большинстве случаев пациенты даже не подозревают о наличии у них той или иной болезни, а в условиях временноݩго цейтнота стоматологического приема врачу получить исчерпывающую информацию о состоянии здоровья пациента крайне трудно. Следовательно, любой пациент, обратившийся за стоматологической помощью, должен рассматриваться врачом-стоматологом как представляющий эпидемиологическую опасность независимо от степени риска заражения!
По мнению участников совещания Неформальной сети по профилактике инфекций и инфекционному контролю в здравоохранении ВОЗ (2008), инфекции, связанные с оказанием медицинской помощи (ИСМП), представляют собой серьезную проблему общественного здравоохранения и значительное бремя для пациентов и медицинских работников, затрагивая все страны [6]. К ИСМП относится внутрибольничная инфекция (ВБИ), которую Европейское бюро ВОЗ определяет как «любое клинически выраженное инфекционное заболевание, которое поражает больного в результате его поступления в медицинское учреждение или обращения в него за лечебной помощью или сотрудников медицинского учреждения вследствие их работы в данном учреждении вне зависимости от появления симптомов заболевания во время или после пребывания в медицинском учреждении» [16].
Из основных групп ВБИ в стоматологии наиболее актуальны инфекции операционных ран и кровотока [6], развивающиеся в результате реализации гемоконтактного механизма передачи (через медицинские манипуляции) или контактного механизма, при котором возбудители, локализующиеся на коже и ее придатках, слизистой оболочке глаз, полости рта, поверхности ран одного пациента, инфицируют другого пациента при их прямом контакте или через обсемененные предметы госпитальной среды. Необходимо помнить о возможности перекрестного инфицирования пациентов и профессионального заражения медицинского персонала в результате реализации воздушно-капельного и контактного механизма передачи инфекции. Вероятные пути передачи инфекции от пациента к пациенту при стоматологических вмешательствах представлены в виде эпидемиологической цепочки (рис. 1, см. на цв. вклейке)
.
Рис. 1. Возможные пути передачи инфекции от пациента к пациенту при стоматологических вмешательствах.
К современным факторам, способствующим росту ВБИ в стоматологической практике, следует отнести:
— сложившуюся эпидемиологическую ситуацию по ВИЧ-инфекции, вирусным гепатитам, герпесвирусным инфекциям и др.;
— распространение потребления парентеральных психотропных препаратов;
— быстрый рост устойчивости микроорганизмов к противомикробным препаратам вплоть до мультирезистентности (например, M. tuberculosis
, грамотрицательные бактерии);
— распространение резистентных штаммов среди пациентов лечебно-профилактического учреждения в отсутствие эффективных программ инфекционного контроля;
— широкое использование инвазивных методов диагностики и лечения;
— создание крупных высокотехнологичных медицинских комплексов со специфической микроэкологией;
— трудности дезинфекции и стерилизации сложной медицинской аппаратуры;
— неблагополучная экологическая обстановка;
— увеличение среди пациентов числа лиц с проявлениями вторичного иммунодефицита.
Описаны экзогенные (первичные) и эндогенные (вторичные) источники инфицирования при стоматологических вмешательствах. При экзогенном инфицировании источником инфекции являются пациенты и медицинский персонал, инфицированные патогенными и условно-патогенными микроорганизмами. Под эндогенным инфицированием следует понимать активацию латентной инфекции под воздействием стрессовых воздействий (страх, обострение хронических заболеваний, ОРВИ и др.) и аутоинфицирование, этиологическими факторами которых в 85% случаев являются представители условно-патогенной флоры [1, 4].
Особого внимания заслуживает эндогенное инфицирование, легкость реализации которого объясняется чрезвычайно богатой аухтонной и аллохтонной микрофлорой слизистой, значительно варьирующейся у разных людей, а также у одного и того же человека в разное время. Представителями аухтонной микрофлоры являются резидентные микроорганизмы (от 160 до 300 видов; до 100 видов может быть выделено из 1 участка, из которых не менее 30 видов — постоянно живущие) и транзиторные микроорганизмы, состав которых зависит от факторов внешней среды (потребляемые продукты и вода, гигиенические процедуры и др.). Представители аллохтонной флоры попадают в полость рта из других микробиоценозов (из кишечника, носоглотки, дыхательных путей и др.). В результате исследований, проведенных в 2003 г. Л.П. Зуевой и соавт., было показано, что более 1/3 больных являются носителями Staphylococcus aureus
, 10% штаммов которого устойчивы к 5 и более антибактериальным препаратам
(рис. 2, см. на цв. вклейке)
.
Рис. 2. Представители микрофлоры полости рта, носа и зева, выявленные у пациентов, обратившихся за стоматологической помощью в отделение челюстно-лицевой хирургии. По результатам многолетних исследований J. Prieto-Prieto, A. Calvo и T. Kuriyama и соавт., в спектре одонтогенных бактерий среди анаэробов преобладают Peptostreptococcus, Prevotella
и
Fusobacterium
, среди аэробов —
Str. viridians(рис. 3, см. на цв. вклейке)
Рис. 3. Спектр одонтогенных бактерий (Kuriyama и соавт., 2002; Prieto-Prieto J., Calvo A., 2004). [13, 19]. По данным А.А. Зорькина и соавт. (2009), наиболее часто при воспалительных процессах в полости рта выявляют
Actinobacillus actinomycetemcomitans
и
Porphyromonas gingivalis
, реже —
Bacteroides forsythus, Prevotella intermedia, Prevotella nigrenscens, Fusobacterium
spp.,
Peptococcus micros, Carnocytophaga
spp.,
Treponema denticola, Treponema sokranskii
. Типичные возбудители одонтогенных инфекций —
Peptostreptococcus
spp.,
Peptococcus
spp.,
Fusobacterium
spp., инфекций пародонта —
A. actinomycetemcomitans, P. gingivalis, Pr. intermedia, Eikenella corrodens, Fusobacterium nucleatum
(особенно при тяжелых инфекциях).
Практикующим врачам важно помнить, что разнообразие микроорганизмов создает уникальные возможности для передачи детерминант вирулентности и резистентности, резервуаром которых является нормальная микрофлора [9, 20]. Описана возможность обмена генетической информацией между бактериями мочеполовых путей и полости рта, а в лабораторных условиях — между таксономически отдаленными видами микроорганизмов [9].
Инфекционные агенты тканей полости рта, от коммесалов до патогенов, играют этиологическую роль не только в запуске стоматологических заболеваний (кариеса, пародонтита, гингивита и др.). Нарушенная при стоматологических процедурах, травмах, инфекциях целостность барьера мягких тканей полости рта приводит к транзиторной бактериемии (фунгемия, виремия) и попаданию микроорганизмов в не свойственные им ткани (например, соединительную ткань, кровь), в результате чего индуцируются системные изменения экспрессии генов, приводящие к повышению вирулентности инфекционных агентов. Становясь эндогенными патогенами, микроорганизмы могут выполнять триггерную роль в формировании патологии пищеварительной, дыхательной, сердечно-сосудистой (ДВС-синдром, инфекционный эндокардит, атеросклероз) систем, ревматизма, нефропатии, многих инфекционно-аллергических состояний, аутоиммунных болезней (ревматоидный артрит — РА, болезнь Бехчета и др.) [10, 11, 20]. Так, доказано, что у S. sanguinis, S. oralis, S. mutans, S. salivarius
достаточно конститутивной экспрессии генов вирулентности, чтобы при попадании в кровоток индуцировать связывание тромбоцитами фибриногена, агрегацию и образование тромба, а при оседании на измененных или аномально развитых клапанах приводить к развитию инфекционного эндокардита. Изменение вирулентности может происходить под действием генов, регулируемых кислотностью среды, в которую попадают микроорганизмы. Так, при повышении pH до 7,3-7,5 у
S. gordonii
возрастает тромбиноподобная активность. При контакте с ламинином и коллагеном поврежденных клапанов сердца
S. gordonii
запускают экспрессию ламининсвязывающего белка, повышающего адгезию бактерий к поверхности клапана [11].
Интересен феномен бактериальной мимикрии у представителей микрофлоры полости рта. Так, сходство эпитопа белка клеточной стенки S. sanguinis
— PAAP, связанного с агрегацией тромбоцитов, с артритогенным эпитопом коллагена типа II, может быть одной из причин развития РА. Образуемый в норме у человека белок теплового шока (HSP60) высокогомологичен бактериальным HSP
Mycobacterium
(HSP65),
S. sanguinis
(HSP65),
Helicobacter pylori
(HSP60). Образующиеся антитела к ним перекрестно реагируют с развитием системной воспалительной реакции и через активацию системы комплемента приводят к иммунному воспалению в стенке сосудов, артриту, болезни Бехчета [14].
На долю инфекционных заболеваний, источником которых могут быть носители «классических» возбудителей (гепатитов, ВИЧ-инфекции, туберкулеза, сифилиса, герпес-вирусов и др.), приходится не более 15% от всей ВБИ медицинских учреждений стоматологического профиля. По данным ВОЗ (2007, 2010) [2, 6], среди всех инфекционных болезней для стоматологов и их пациентов наиболее актуальны вирусные гепатиты A, В, С, Д (TTV, G, SEN — ?), ВИЧ-инфекция, герпесвирусная инфекция, туберкулез, кандидозы, ОРВИ и грипп, корь, легионеллез, эпидемический паротит, стрептококковые болезни (ангина, скарлатина), стафилококковые (ангина, пневмония, энтероколит, гнойные поражения кожи и подкожной клетчатки и др.), дифтерия, сифилис, гонорея и столбняк. Основные инфекционные заболевания, имеющие клинические проявления в полости рта, представлены в таблице
.
Следует признать, что проявления даже хорошо известных инфекционных болезней могут меняться на фоне хронических заболеваний пациента или при ко-инфицировании, приобретая несвойственные им черты, что затрудняет их клиническую диагностику и требует своевременного лабораторного обследования.
Кроме представленных в таблице
инфекционных заболеваний, существует обширная группа вирусных инфекционных болезней, не имеющих характерных патологических проявлений в полости рта, но передающихся гемоконтактно при стоматологических вмешательствах, что ведет к развитию угрожающих жизни заболеваний пациентов и медицинского персонала (вирусный гепатит В, С, Д; цитомегаловирусная инфекция; Эпштейна-Барр вирусная инфекция — кроме описанных выше инфекционного мононуклеоза и опоясывающего герпеса; герпесвирусная инфекция, вызванная HHV-6, HHV-7, HHV-8 типом, и др.).
Все вышесказанное свидетельствует о большой роли инфекционных агентов в патологии человека в целом и в стоматологической практике, в частности. Врач-стоматолог в любой момент может встретиться с инфекционным больным. От его эрудиции и знаний нередко зависят жизнь пациента и своевременное пресечение эпидемического процесса, позволяющее предупредить перекрестное заражение и инфицирование медицинского персонала при оказании стоматологической помощи.
НЕОДОНТОГЕННАЯ И СПЕЦИФИЧЕСКАЯ ИНФЕКЦИЯ
НЕКРОТИЧЕСКИЙ СТОМАТИТ (ЯЗВЕННО-НЕКРОТИЧЕСКИЙ ГИНГИВОСТОМАТИТ ВЕНСАНА)
Основные возбудители
В десневой бороздке концентрируются Fusobacterium
, пигментированные
Bacteroides
, анаэробные спирохеты. При некротическом стоматите имеется тенденция к быстрому распространению инфекции в окружающие ткани.
Возбудителями являются F.nucleatum, T.vinsentii, P.melaninogenica, P.gingivalis и P.intermedia
. У пациентов со СПИДом частым возбудителем гингивита является
C.rectus
.
Выбор антимикробных препаратов
Препараты выбора:
феноксиметилпенициллин, пенициллин.
Альтернативные препараты:
макролид + метронидазол.
Длительность терапии:
в зависимости от тяжести течения.
АКТИНОМИКОЗ
Основные возбудители
Основным возбудителем актиномикоза является A.israelii
, также возможна ассоциация с грамотрицательными бактериями
A.actinomycetemcomitans
и
H.aphrophilus
, которые устойчивы к пенициллину, но чувствительны к тетрациклинам.
Выбор антимикробных препаратов
Препараты выбора
: пенициллин в дозе 18-24 млн ЕД/сут, при положительной динамике — переход на ступенчатую терапию (феноксиметилпенициллин 2 г/сут или амоксициллин по 3-4 г/сут).
Альтернативные препараты
: доксициклин 0,2 г/сут, пероральные препараты — тетрациклин 3 г/сут, эритромицин 2 г/сут.
Длительность терапии
: пенициллин 3-6 нед в/в, препараты для приема внутрь — 6-12 мес.